La rehabilitación tras un ictus isquémico agudo suele aplicarse con protocolos relativamente estandarizados, pero la respuesta clínica real no es homogénea: hay pacientes que mejoran de forma clara y otros que apenas cambian. Este artículo no pretende responder “cuánto ayuda la acupuntura en el ictus” en términos generales, sino dar un paso distinto: construir una herramienta que permita identificar de forma temprana qué pacientes tienen más probabilidad de beneficiarse cuando se integra acupuntura en el contexto hospitalario de rehabilitación.
Los autores, Zhao L et al. (Front Neurol. 2025) parten de dos ideas. La primera es que existen modelos pronósticos de ictus basados en variables clínicas convencionales (edad, antecedentes, analítica), pero esos modelos tienen un límite: describen al paciente “por fuera” y no siempre capturan detalles específicos de la lesión cerebral. La segunda es que la radiómica permite extraer de forma masiva (high-throughput) características cuantitativas de la imagen que no son distinguibles a simple vista y que pueden reflejar, con mayor granularidad, heterogeneidad tisular y cambios patofisiológicos. Con esa lógica, proponen un modelo multimodal clínica+radiómica que intente predecir “respuesta” a acupuntura.
El estudio es retrospectivo y unicéntrico. Incluye 186 pacientes con ictus isquémico agudo ingresados entre enero de 2022 y diciembre de 2024 en el Hospital de la Universidad de Medicina Tradicional China de Liaoning. Se incluyeron adultos (≥18 años) con infarto cerebral de novo confirmado por MRI con DWI antes del tratamiento, que recibieron acupuntura durante la hospitalización y tenían Barthel Index (BI) registrado al ingreso y al alta. Se excluyeron, entre otros, hemorragia, tumor cerebral, mala calidad de imagen y comorbilidad grave que pudiera interferir.
La intervención de acupuntura se describe de forma bastante concreta: acupuntura corporal diaria, en decúbito supino, con agujas estériles desechables 0,25×40 mm, técnicas de manipulación para obtener deqi y retención 30 minutos. Los puntos seleccionados fueron LI4, PC6, LU5, LI11, GB34, SP9, GB31, ST36, SP6 y LV3. Este detalle importa porque el modelo, si funciona, sería válido sobre todo para contextos clínicos que se parezcan a este protocolo (frecuencia diaria, selección de puntos y práctica hospitalaria concreta).
El desenlace principal no es una escala neurológica clásica a 90 días como la mRS, sino el cambio funcional durante el ingreso medido por Barthel Index. Definen ΔBI = BI al alta − BI al ingreso. Consideran “respondedor” (grupo eficaz) a quien tiene ΔBI>0 y “no respondedor” (ineficaz) a quien tiene ΔBI≤0. Los BI fueron evaluados por profesionales entrenados y en ventanas temporales estandarizadas: dentro de las 24 horas del ingreso y dentro de las 24 horas previas al alta, con entrenamiento para reducir variabilidad entre evaluadores. En la cohorte, 103 pacientes quedaron clasificados como “eficaces” y 83 como “ineficaces”.
Conviene detenerse aquí en la interpretación clínica: este diseño permite predecir quién tiende a mejorar funcionalmente durante la hospitalización en un escenario donde todos reciben acupuntura, pero no separa de forma estricta qué parte de esa mejoría es atribuible específicamente a la acupuntura frente a la evolución natural, cuidados médicos, fisioterapia u otras intervenciones concomitantes. Los autores justifican su enfoque como un intento de medir un indicador “relacionado con la intervención” (ΔBI) y trasladar el foco desde el pronóstico global del ictus hacia la respuesta a una intervención concreta. Ese es el salto conceptual del trabajo, aunque debe leerse con cautela metodológica.
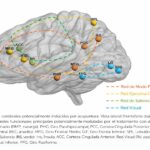
En los datos clínicos recogieron un conjunto amplio de variables: edad, sexo, factores de riesgo (hipertensión, diabetes, dislipemia, cardiopatía), antecedentes (incluida historia de ictus), hábitos, hemograma, lípidos, glucemia, presencia de infartos múltiples, otros tratamientos de rehabilitación y BI pre y post. Posteriormente dividieron aleatoriamente la muestra en entrenamiento (n=126) y prueba (n=60) con proporción 7:3. Un detalle relevante es que reportan diferencias estadísticamente significativas en edad y “days of illness” entre los grupos dentro de entrenamiento y prueba (p<0,05), lo que sugiere que los conjuntos no quedaron perfectamente equilibrados en variables potencialmente influyentes. La parte de imagen se centró en MRI con difusión (DWI, b=1000 s/mm²) en un escáner Philips 3.0T. Las lesiones se segmentaron manualmente: un radiólogo adjunto con 5 años de experiencia delineó las regiones de interés siguiendo los bordes del infarto; en casos con múltiples infartos se delinearon todas las lesiones visibles, incluidas pequeñas lesiones dispersas, y un segundo especialista confirmó las segmentaciones. Las ROIs se importaron anonimizadas a 3D Slicer (v4.10.2) y se extrajeron 851 características radiómicas, incluyendo primer orden (histograma), forma y matrices de textura (GLCM, GLDM/DIDM, GLSZM, GLRLM, NGTDM), además de características derivadas por wavelets. El reto clásico de la radiómica aparece de inmediato: 851 variables son muchísimas para 186 pacientes, lo que eleva el riesgo de que un algoritmo “memorice” patrones del conjunto y rinda bien en entrenamiento, pero falle fuera. Para controlar esto, aplicaron un pipeline de selección de características: primero normalización min–max para escalar variables a [0,1]; después un filtro por correlación de Pearson para reducir redundancia; y finalmente LASSO con validación cruzada 10-fold para seleccionar los predictores más informativos. En lenguaje sencillo, LASSO actúa como un “filtro con penalización” que apaga variables poco útiles y ayuda a evitar sobreajuste, mientras que la validación cruzada intenta que la selección no dependa de un único corte del dataset. Tras la selección, el modelo clínico retuvo cuatro variables: edad, days of illness, historia de ictus e hipertensión. Los autores interpretan estas variables como reflejos del estado fisiológico basal, de la ventana temporal de intervención y de la carga vascular previa. En discusión especifican que “days of illness” se entiende como días desde el inicio hasta la primera sesión de acupuntura, destacando el componente de oportunidad temporal en fase aguda. El modelo radiómico retuvo ocho características: una morfológica (original_shape_MajorAxisLength) y siete de textura (combinaciones GLRLM/GLDM/GLSZM/NGTDM, muchas en dominios wavelet). Reportan el listado completo y muestran un ranking por importancia basado en el valor absoluto de los coeficientes del LASSO. La interpretación clínica que proponen es que estas características cuantifican tamaño/extendibilidad espacial, heterogeneidad microscópica y patrones de compartimentación de intensidades (“alto/bajo gris”) dentro del infarto, aportando una “capa” de información que no se obtiene solo con variables clínicas. Con estas variables construyeron tres familias de modelos: uno clínico, uno radiómico y uno combinado (clínica+radiómica). Compararon tres algoritmos de aprendizaje automático: regresión logística (LR), LightBoost y KNN. La evaluación del rendimiento incluyó AUC (área bajo la curva ROC), accuracy, sensibilidad, especificidad, precisión y F1. También compararon AUC mediante test de DeLong. En paralelo, evaluaron calibración y utilidad clínica mediante curvas de calibración (Hosmer–Lemeshow p>0,05) y decision curve analysis (DCA).
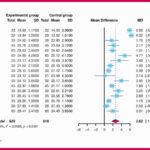
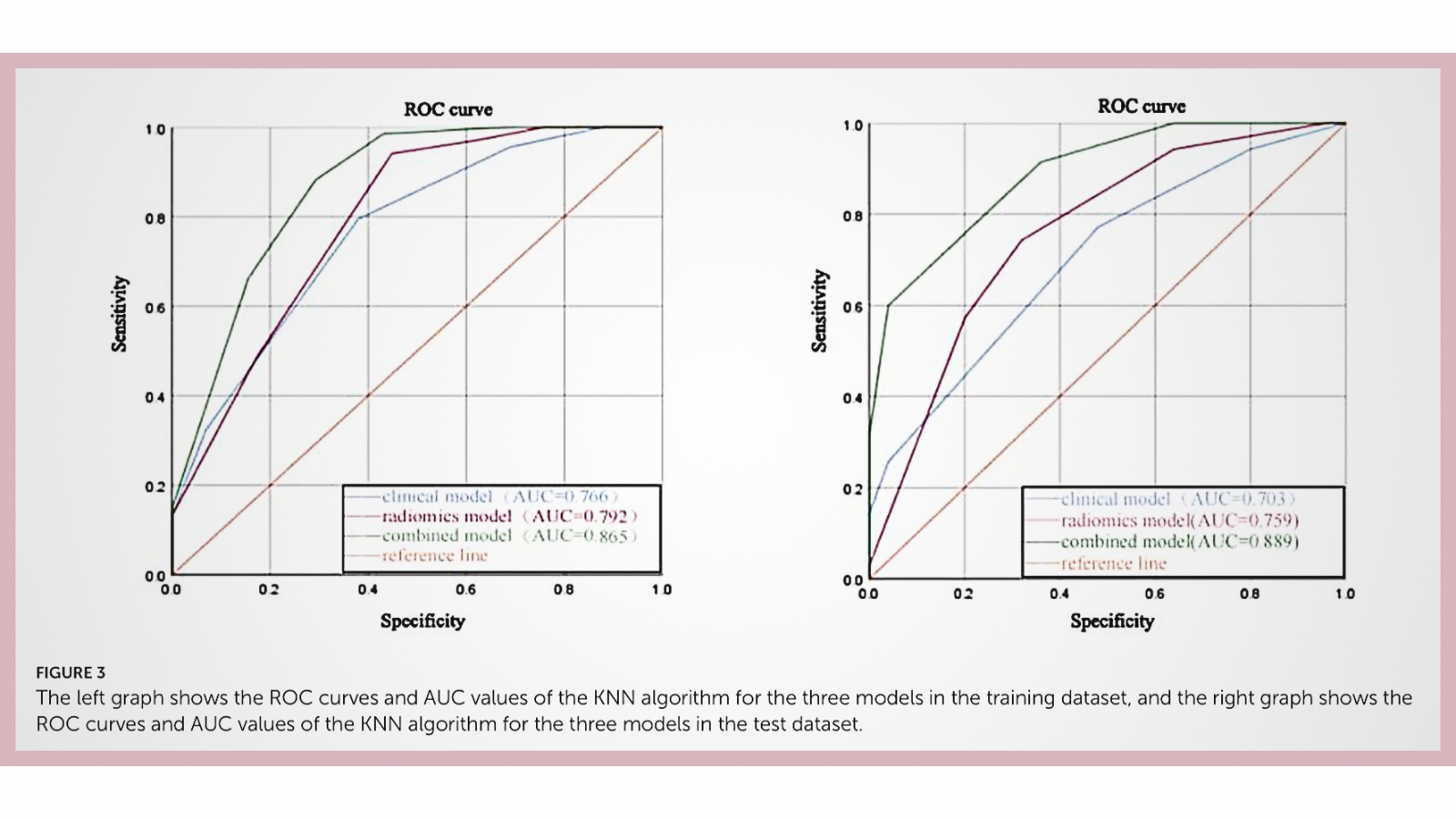
La tabla de resultados resume bien el mensaje principal. En el conjunto de prueba, el modelo clínico ofrece rendimiento limitado (AUC aproximadamente 0,689–0,703 según el algoritmo), el modelo radiómico mejora moderadamente (AUC 0,729–0,759), y el modelo combinado es el que alcanza mayor discriminación, especialmente con KNN. Con KNN, el modelo combinado obtuvo AUC 0,889 (IC95% 0,809–0,968), accuracy 0,800, sensibilidad 0,914 y especificidad 0,640, con precisión 0,781 y F1 0,842. En términos prácticos, el modelo identifica a la mayoría de respondedores (alta sensibilidad) pero comete un número relevante de falsos positivos (especificidad moderada), algo que los propios autores discuten en clave de riesgo de sobretratamiento y necesidad de optimización futura.
Para un lector sin formación en machine learning, dos ideas ayudan a interpretar estas métricas sin perderse. La primera es que el AUC indica qué tan bien el modelo “ordena” a los pacientes: cuanto más cerca de 1, mejor discrimina entre respondedor y no respondedor. La segunda es que sensibilidad y especificidad describen el tipo de error: alta sensibilidad reduce el riesgo de “dejar fuera” a alguien que sí podría beneficiarse, mientras que una especificidad moderada implica que algunos pacientes serán clasificados como “respondedores probables” cuando en realidad no lo son. En un contexto clínico, la aceptabilidad de ese balance depende del coste, disponibilidad y perfil de riesgos de la intervención, además de la posibilidad de combinarlo con otras decisiones terapéuticas.
La calibración y la DCA aportan una capa más aplicada. La calibración responde a si las probabilidades predichas se parecen a lo que realmente ocurre (por ejemplo, si el modelo da 70% de respuesta, que aproximadamente 7 de cada 10 respondan). La DCA intenta traducir la predicción a beneficio neto clínico en distintos umbrales de decisión. En el artículo se reporta que los modelos KNN pasan Hosmer–Lemeshow con p>0,05 y que el combinado ofrece mayor beneficio neto en un intervalo de umbrales razonable. Estas herramientas son relevantes porque un modelo puede tener AUC aceptable y aun así ser poco útil si no calibra bien o si no mejora decisiones reales.
En la discusión, se subraya como innovación el cambio de foco: en lugar de predecir el pronóstico global del ictus (que refleja curso natural y tratamiento integral), intentan predecir la respuesta a una intervención de rehabilitación concreta, dotando al modelo de un componente “theranostic”. Plantean una posible utilidad práctica: si el modelo predice alta probabilidad de respuesta, se podría priorizar acupuntura; si predice baja probabilidad, se podría reorientar antes hacia otras estrategias o combinaciones. Este razonamiento es conceptualmente atractivo para medicina personalizada y asignación de recursos, aunque su traslación clínica exige validación más sólida.
Las limitaciones reconocidas por los autores son importantes y deben acompañar cualquier interpretación. Se trata de un estudio unicéntrico, retrospectivo, con tamaño muestral moderado y sin validación externa; esto limita la generalización y aumenta el riesgo de que el rendimiento sea optimista fuera del hospital donde se entrenó. La segmentación manual puede introducir sesgo y variabilidad, por lo que proponen explorar segmentación automática basada en deep learning en trabajos futuros. Además, aunque incluyeron la variable “otros tratamientos de rehabilitación”, el desenlace ΔBI durante el ingreso sigue siendo sensible a factores como intensidad de fisioterapia, cuidados interdisciplinarios o duración de estancia, elementos que pueden actuar como confusores cuando se interpreta “respuesta a acupuntura” sin un comparador sin acupuntura.
Leído con equilibrio, el artículo aporta una idea valiosa para la acupuntura clínica en ictus: la pregunta relevante no siempre es solo “funciona o no funciona”, sino “en qué pacientes tiene más sentido esperar beneficio”, y cómo objetivar esa selección usando información clínica y de neuroimagen. En este trabajo, la combinación de cuatro variables clínicas (edad, hipertensión, historia de ictus y días desde inicio a primera acupuntura) con ocho características radiómicas de DWI produjo el mejor rendimiento interno con KNN. El siguiente paso necesario, para que el enfoque sea realmente clínicamente aplicable, es replicar el modelo de forma prospectiva, multicéntrica y con validación externa, idealmente con diseños que permitan separar mejor la mejoría global del ingreso de la contribución específica de la intervención.
Referencia:
Zhao L, Huang Z, Zhao B, An R, Cheng Y. Prediction of acupuncture efficacy in acute ischemic stroke constructing a clinical-radiomics multimodal model. Front Neurol. 2025 Nov 28;16:1682842. doi: 10.3389/fneur.2025.1682842. PMID: 41393999; PMCID: PMC12698441.
 Fuente
Fuente Dr. Beltran Carrillo
Dr. Beltran Carrillo